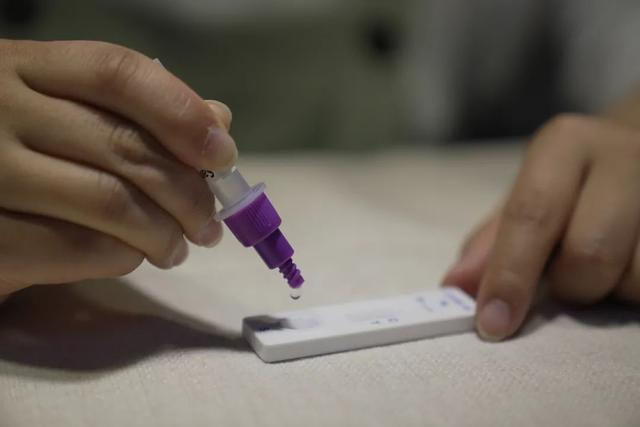
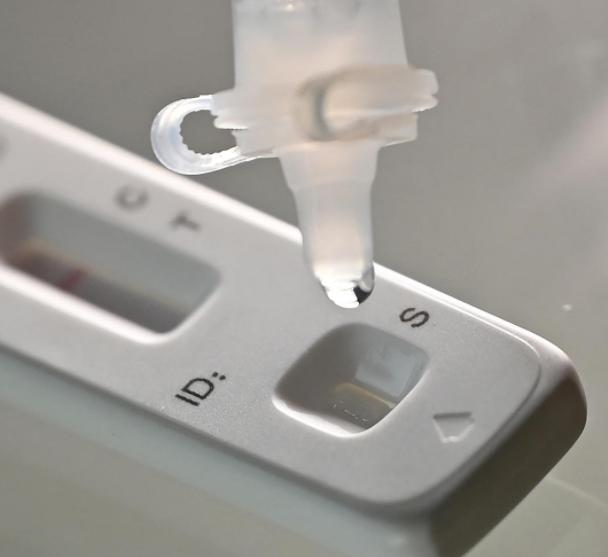
Il 12 marzoth 2022, ilNMPA (SFDA) ha emesso un avviso di approvazione della modifica della domanda di autotest dei prodotti antigenici COVID-19 da parte di Nanjing Vazyme BiotechCo., Ltd, Tecnologia di bioingegneria di Pechino JinwofuCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd eBeijing Savant Biotechnology Co., ltd(Huaketai).Sono stati lanciati cinque prodotti per l'autotest dell'antigene COVID-19.
L'11 marzo 2022, l'NHC aveva annunciato che, al fine di ottimizzare ulteriormente la strategia di test del Nuovo Coronavirus e soddisfare le esigenze di prevenzione e controllo del COVID-19, il Gruppo completo del meccanismo congiunto di prevenzione e controllo del Consiglio di Stato ha deciso di aggiungere test dell'antigene al test dell'acido nucleico e realizzato "il protocollo di applicazione per il rilevamento (trial) dell'antigene del nuovo coronavirus"
Il protocollo specifica la popolazione applicabile per il test dell'antigene:
In primo luogo, coloro che visitano le istituzioni mediche di base e presentano sintomi come le vie respiratorie e la febbre entro 5 giorni dall'insorgenza dei sintomi;
In secondo luogo, il personale di osservazione della quarantena, compreso l'osservazione della quarantena domestica, il contatto ravvicinato e il sub-contatto ravvicinato, l'osservazione della quarantena all'ingresso, l'area di contenimento e il personale dell'area di controllo;
Il terzo sono i residenti della comunità che hanno bisogno dell'autorilevamento dell'antigene.
Suggerimenti: il rilevamento dell'antigene è un supplemento importante del rilevamento dell'acido nucleico, ma i risultati dell'autorilevamento dell'antigene non possono essere utilizzati come base per la diagnosi dell'infezione
Tempo di pubblicazione: 22 marzo 2022